|
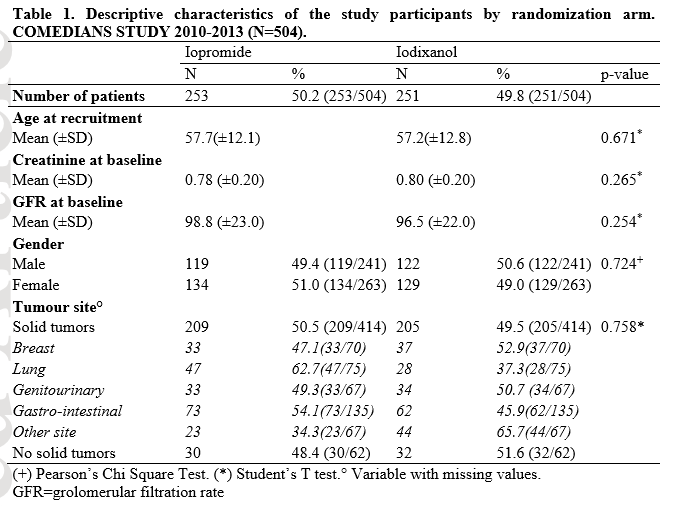
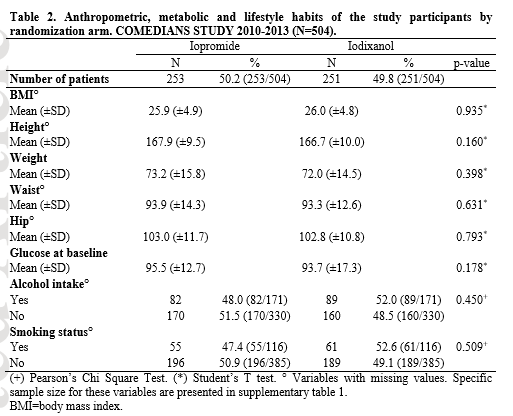
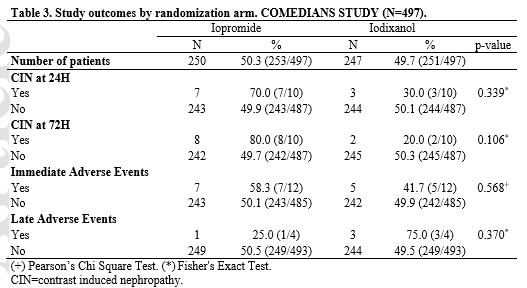
威视派克肾脏安全性再添新证据 低风险癌症患者对比剂应用肾脏安全性对比研究 癌症患者中碘克沙醇vs碘普罗胺:来自随机临床研究的证据 (Iodixanol vs iopromide in cancer patients: evidence from a randomized clinical trial) 研究背景: 对比增强计算机断层扫描(CT)是癌症患者管理中使用最多的成像技术之一,其可以进行诊断、疾病分期、疗效评估和中长期随访。对比剂肾病(CIN)是一种多因素综合征,且癌症患者发病率更高。在癌症治疗方面,化疗现在是结构化治疗策略的一部分,其对CIN进展的影响需要全面评估。然而,在近期更新的CIN预防共识指南中,明确指出化疗对肾功能的影响,其中化疗被列为肾损伤和CIN进展的风险因素之一。在CT扫描过程中使用的对比剂(CM)的特征则是需要考虑的辅助因素。到目前为止,没有证据支持在癌症患者中使用特定的CM。鉴于其安全性和患者耐受性,特别是对于动脉内注射,通常优选使用等渗CM。类似地,静脉内(iv)途径的等渗vs低渗CM研究结果也是支持等渗CM的使用,因为其不适感更少、更为安全,且在肝、主动脉和门静脉中增强效果更好。在CT扫描过程中含碘CM给药后CIN的试验中已经反复考虑了基于估计的肾小球滤过率(eGFR)的单一患者水平上的CIN发生风险,但其结果不一致。基线eGFR对静脉内CM给药与CIN进展之间因果关系的影响仍有争议。 目的: 评估eGFR>60 ml/min的癌症患者(进行含碘对比剂的胸部-腹部-骨盆CT)中,等渗CM vs低渗CM的安全性。 结论:研究结果表明,与碘普罗胺相比,碘克沙醇更为安全。应该设计纳入足够受试者的相似设计的试验进一步证实该研究发现,并阐明潜在的生物学机制。 材料和方法: 在这项多中心、设盲、随机临床试验中,根据预先确定的标准筛选患者资格。在基线处收集静脉血样20ml,以评估eGFR、血清肌酐(Scr)和血细胞比容,后者被认为是水合的代表。符合条件的受试者按照1:1的比例随机分配接受碘克沙醇或碘普罗胺。以4ml/s速率给予两组相对于体重(0.55g/Kg)的等效剂量的碘。以1.73ml/kg剂量给药碘克沙醇(320mg/ml),以1.5ml/kg剂量给药碘普罗胺(370mg/ml)。研究对患者和护士设盲,而药理学家、放射科医师、技术人员和统计学家对分组情况明确。主要结局指标是24和/或72h时CIN进展(CIN定义为基线eGFR>25%的降低。为了评估CIN进展,研究人员还考虑了Scr水平。关于Scr,CIN病例定义与基线相比绝对升高0.5mg/d或相对升高>25%)。次要结局指标为不可逆的CIN进展(即至少15天持续CIN)、两个研究组之间平均GFR百分比变化(GFR%Δ)和与CM使用相关的任何短期、长期不良事件(AEs)。 结果:总共有607例患者入组,鉴于血清样本的基线评估结果,排除了84例患者,后19名患者撤回入组同意。在剩余的504名患者中,7名患者的数据不可用。因此,随机分组描述性统计学结果与504名癌症患者相关,而对497名参与者进行了结局分析。(具体见Figure 1)。表1(table 1)总结了随机分组的研究参与者特征。表2(table 2)比较了两个研究组的人体测量学,即身体质量指数(BMI)、身高、体重、臀围等。497名符合纳入标准的患者被随机分配接受碘克沙醇(N:247)或碘普罗胺(N:250)。描述性特征没有出现差异。表3(table 3)报告了主要结局指标和次要结局指标。碘普罗胺和碘克沙醇组在24小时分别发生7例和3例CIN(p=0.34),72小时分别发生8例和2例CIN(p=0.11)。在进展CIN(N:17)的个体患者亚组中,碘普罗胺组的事件率较高(p=0.045)。没有观察到永久性CIN病例或AEs或GFR%Δ的显著差异。 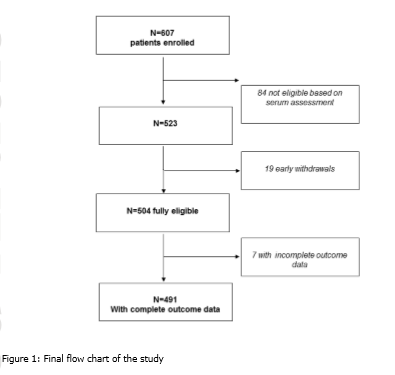
讨论:研究中两组CIN事件的分布似乎表明,因为更有利的毒性特征支持使用碘克沙醇。在区别早期和晚期发生的CIN事件时,与碘克沙醇组相比,碘普罗胺组的事件率较高。该研究结果与既往公布的RCTs数据比较一致。既往RCTs表明,与低渗CM相比,碘克沙醇记录了较少的患者不适、较少的AEs频率和相当或更高质量的图像。该研究结果值得关注的重点是CIN进展风险很低的癌症患者以及研究设计,即多中心、设盲、随机、临床研究。事实上,据我们所知,既往关于癌症患者CIN的数据通常来自观察性研究,其规模、设计和参与者的特征极其不同。一些注意事项来源于文献综述。关于感兴趣主题的证据正在显著增长,而且远远不能产生相当一致的数据,这些观察性研究本质上容易产生偏见和混淆。在此基础上,适当规模、随机临床试验的设计和实施可大大提高癌症患者中CIN进展的科学证据质量。总之,研究人员设计并实施了一项多中心、设盲临床试验,将CIN进展低风险进行胸腹部CT的癌症患者随机分配接受碘克沙醇或碘普罗胺。在评估主要结局指标时,即CM给药24和72小时的CIN进展,研究人员未观察到研究组间统计学上的相关差异。然而,与碘普罗胺相比,研究结果对于碘克沙醇的安全性更为有利。在分析剩余结局的数据时,没有观察到相关差异。 文章及作者信息: Received 1 August 2017; Accepted 3 August 2017 Journal of Cellular Physiology This article is protected by copyright. All rights reserved DOI 10.1002/jcp.26132 Irene Terrenato1* PhD, Francesca Sperati1* PhD, Felice Mussicco2 PharmD, Anna Fausta Pozzi3 PharmD, Annunziata di Turi4 PhD, Mauro Caterino5 MD, Elisabetta de Lutio di Castelguidone6 MD, Sergio Venanzio Setola6 MD, Massimo Bellomi7,8 MD, Carlo Emanuele Neumaier9 MD, Laura Conti10 MD, Giovanni Cigliana10 PhD, Roberta Merola10 PhD, Anna Antenucci10 PhD, Giulia Orlandi10 PhD, Antonio Giordano11,12 MD, PhD, Maddalena Barba4,13** MD and Stefano Canitano5 MD. 1: Biostatistic Unit, Regina Elena National Cancer Institute, Rome, Italy. 2: Service of Pharmacovigilance, Regina Elena National Cancer Institute, Rome, Italy. 3: AUSL di Bologna, Bologna, Italy. 4: Scientific Direction, Regina Elena National Cancer Institute, Rome, Italy. 5: Department of Diagnostic Imaging, Regina Elena National Cancer Institute, Rome, Italy. 6: Department of Diagnostic Imaging, radiant and metabolic Therapy, Istituto Nazionale Tumori IRCCS Fondazione Pascale, Naples, Italy. 7: Department of Medical Imaging and Radiation Sciences, European Institute of Oncology, Milan, Italy. 8: Department of Oncology and Hematology-Oncology, University of Milan, Milan, Italy. 9: Diagnostic Imaging and Senology, IRCCS-A.O.U., San Martino-IST, Genoa, Italy. 10: Departement of Clinical Patology, Regina Elena National Cancer Institute, Rome, Italy. 11: Department of Medicine, Surgery and Neuroscience, University of Siena and Istituto Toscano Tumori & #40;ITT& #41;, Siena, Italy. 12: Sbarro Institute for Cancer Research and Molecular Medicine, Department of Biology, College of Science and Technology, Temple University, Philadelphia PA, USA. 13: Division of Medical Oncology 2, Regina Elena National Cancer Institute, Rome, Italy.
|