|

本期作者 李昕 博士 GE Healthcare Life Sciences Core-Imaging药代动力学研究中心(PKRC)成员 专业领域: Medical Imaging, Medical Image Processing and Machine Learning 研究方向: 肿瘤异质性分析,肿瘤影像相关预测模型及机器学习算法研究, 负责k-Series模型构建和平台设计,影像组学,DCE-MRI, CT灌注相关科研开展等。 药代动力学科研平台O.K.,C.K.,A.K. 及相关模型算法主要开发者。 放射组学(Radiomics),又被称为影像组学是新兴的一门以定量成像技术为基础的学科方向,它利用了若干影像特征直观,定量的描述了医学影像中病灶的形态和病理特征。已经有众多研究者开始关注影像组学,尤其是影像组学具有对治疗效果,预后以及疾病遗传因素有较强的预测作用,这些应用也构成了精准医疗的基础。本文主要从宏观上分析了影像组学的研究进展以及当前面临的挑战,同时根据影像组学的图像处理的流程,给出了影像组学在研究中的设计方法。 影像组学的核心是根据获取的图像提取出相关病灶的特征信息,同时利用这些特征信息来直观的,定量的描述病灶的病理和生理特征。图1描述了影像组学的一个简单的实现流程和框架,简单的可以分为特征部分和预测模型部分。首先根据获取的图像,利用数学方法和模型提取出直观肉眼不能描述的特征,如形状大小特征& #40;shape/size feature& #41;,直方图特征& #40;histogram based feature& #41;,滤波特征& #40;fiter-based feature& #41;以及纹理特征& #40;texture feature& #41;等;随即通过模型训练的方法将病理或者基因结果和特征相比较,就构成了一个简单的Radiomics的流程框架。其中上述的特征部分又可以分为特征提取,特征选择,特征表达,模型部分可以分为模型训练以及模型预测。 
图1 影像组学研究的流程 影像组学在研究中的应用 影像组学已经被广泛用于对不同疾病病灶的研究,其中以肿瘤病灶研究较多。影像组学不仅可以从形态学和纹理角度来揭示肿瘤的形态,同时它在肿瘤临床应用中有很大的潜力。例如影像组学对放化疗评估,肿瘤分级,良恶性辨别以及基于基因的肿瘤分类上都有着较强的预测能力,下文姜从几个方面给出临床上影像组学的若干应用。 放化疗的疗效评估预测应用 放化疗的疗效评估是衡量治疗方案,评估临床决策的有效手段,这里我们介绍一些常见的利用影像组学中的特征来进行疗效评估的应用。很多研究给出了MR在放化疗效评估中,使用基于直方图(histogram-based feature)特征的影像组学方法给出较高预测率的实例,如图2所示的一例脑肿瘤的放疗疗效评估研究中,文章使用MRI动态增强图像,结合DCEMRI分析方法,比较了治疗前后的血液动力学参数和直方图参数的相关性和差异,图中可见治疗前后的直方图和峰度(kurtosis)具有较强相关性。

图2 肿瘤治疗前后定量分析 同时在动物实验中,使用临床前模型对患有恶性肉瘤的小鼠进行ADC图像的扫描,发现治疗前后肿瘤区域ADC值的直方图特征,如偏度(skewness),峰度(kurtosis),熵(entropy)均有显著性的差异;利用直方图参数评估头颈部肿瘤的放化疗效果过程中,较差疗效结果相对良好的放化疗效,其ADC图像中肿瘤部位往往呈现较高的峰度和偏度值;同时也有研究将DCEMRI血液动力学模型计算的参数-KTrans作为特征计算的图像,其中KTrans的偏度(Skewness)被发现可以作为中晚期头颈部肿瘤的整体存活率的有效评估依据。 肿瘤细胞分化程度研究 肿瘤细胞分化程度的研究在在临床中具有很重要的意义,它可以提供给临床诊疗决策和影响治疗方案的制定,这里我们也介绍若干影像组学在肿瘤分级上的应用。以往的众多研究中显示,影像组学的特征对早期和较晚期的肿瘤表现出良好的分辨能力,例如在基于PET图像的食管癌分级研究中,SUV-max,Entropy,energy都在辨别早期和中晚期肿瘤中具有显著性的差异,尤其是熵(entropy)达到一定阈值后对鉴别二期肿瘤有着相关性较高的结果;同时有研究发现,在宫颈癌的分级研究中,基于PET图像的步长矩阵纹理特征(RLM)可以很好的鉴别早期肿瘤(I,II期)和晚期肿瘤(III,IV期);在肺癌分级研究中,基于CT图像的高斯滤波纹理特征对鉴别II期以上的肿瘤有着良好的分辨能力。 肿瘤良恶性辨别应用 影像组学中的特征可以在很多临床应用中鉴别肿瘤的良恶性(见图3),从而可以对临床的决策起到指导作用。上世纪90年代,有研究报告基于灰度共生矩阵(GLCM)的纹理特征在分析二维的T1,T2 MRI图像时,可以通过GLCM的到的参数辨别脑部各个区域的肿瘤良恶性;除了组学参数在脑部的应用,在其他部位例如乳腺肿瘤的良恶性辨别上,影像组学也有非常多的应用,例如08年的一例研究中,研究者结合基于形状的纹理参数(shape-based),共生矩阵纹理参数(GLCM)以及三维纹理(volume),利用人工神经网络(ANN)作为训练方法,得到了鉴别率较高的乳腺肿瘤良恶性辨别模型,下图表示了基于直方图(Histogram)的参数 - Gray Level Sum Average对乳腺肿瘤良恶性辨别的例子,蓝色的区域表示良性的肿瘤分布在level较低的区域,红色区域表示恶性的区域。 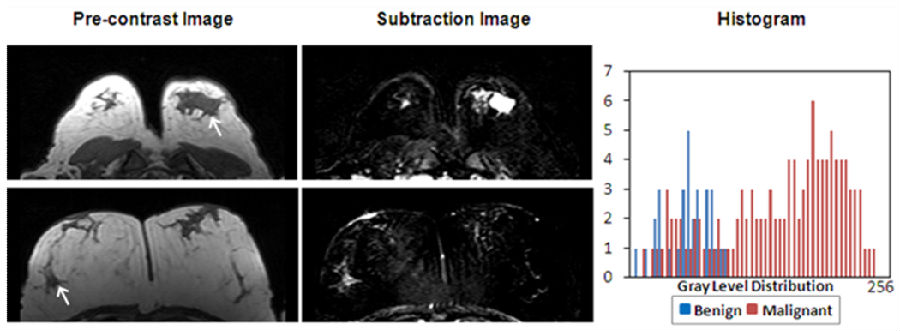
图3 影像组学研究在肿瘤鉴别诊断应用 肿瘤遗传学应用 很多研究发现在肿瘤病理学与肿瘤基因之间存在着很强的关联(见图4),所以研究肿瘤遗传学可以给肿瘤诊断提供生物学方面的基础,影像组学恰好就是病理学与基因学之间的很好结合,可以作为肿瘤遗传学研究的重要手段。在脑部肿瘤遗传学的研究中,通常利用MRI影像中的三维特征与体细胞基因突变,基因表达结合来评估用于遗传学研究,例如2013年的一份研究中指出,不同恶化程度的胶质瘤类型具有不同的三维(volume)纹理特征;在最近的一份研究中,基于容积纹理(volumetric measurements)的参数,例如对比增强容积(contrast enhanced volume),梗死容积(necrosis volume)以及整体肿瘤容积(total tumor volume)被发现对恶性胶质瘤突变类型有着很好的预测效果;在CT图像评估领域中,2014年的一项研究中发现,影像组学的参数特征-形状特征(shape feature)和小波特征(wavelet feature)在描述肿瘤异质性的同时,也对肿瘤细胞的生存周期有着很好的描述,研究最后指出,通常高度增生的肿瘤细胞具有较复杂的图像特征,例如纹理特征等。 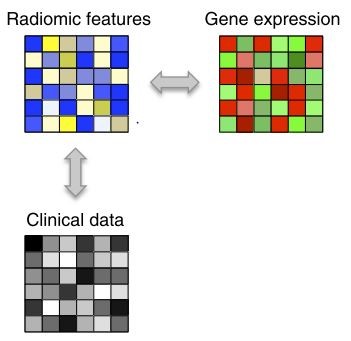
图4 影像组学在遗传性疾病研究中应用 影像组学除了在上述的临床应用中起着非常重要的作用,在其他的应用中同样也有一些应用,总之影像组学作为刚刚兴起的前沿学科,由于它将影像,病理、分子病理与基因信息紧密的联系在一起,利用工程学的方法提供了一整套用于临床决策和科研的解决方案,影像组学在临床应用中将会起到越来越重要的作用。 参考文献 马莉,范影乐 著 纹理图像分析 科学出版社 2009年 北京 Kumar V, Gu Y, Basu S, et al: Radiomics: The process and the challenges. Magn Reson Imaging 30:1234-1248, 2012 McGranahan N, Swanton C: Biological and therapeutic impact of intratumor heterogeneity in cancer evolution. Cancer Cell 27:15-26, 2015 [Erratum: Cancer Cell 28:141, 2015] Aerts HJ, Grossmann P, Tan Y, et al: Defining a radiomic response phenotype: A pilot study using targeted therapy in NSCLC. Sci Rep 6:33860, 2016 Solomon CJ, Breckon TP: Fundamentals of Digital Image Processing: A Practical Approach with Examples in Matlab.Hoboken, NJ, Wiley-Blackwell, 2010 Kessler LG, Barnhart HX, Buckler AJ, et al: The emerging science of quantitative imaging biomarkers terminology and definitions for scientific studies and regulatory submissions. Stat Methods Med Res 24:9-26, 2015 Katrib A, Hsu W, Bui A, et al: “Radiotranomics”: A synergy of imaging and tranomics in clinical assessment.Quant Biol 4:1-12, 2016 Mazurowski MA: Radiogenomics: What it is and why it is important. J Am Coll Radiol 12:862-866, 2015 Calderwood SK: Tumor heterogeneity, clonal evolution, and therapy resistance: An opportunity for multitargeting therapy. Discov Med 15:188-194, 2013 Coroller TP, Agrawal V, Narayan V, et al: Radiomic phenotype features predict pathological response in non-small cell lung cancer. Radiother Oncol 119:480-486, 2016
|